

O Globo | Pollyanna Bretas | 24/09/2023 | Rafael Robba Read more »

Uma moradora de São Caetano, em São Paulo, foi uma das pessoas diagnosticadas com a doença. Com fortes dores abdominais, ela realizou uma série de exames, que indicaram uma extensa carcinomatose peritoneal. Enquanto iniciava o tratamento quimioterápico prescrito por seu médico, ela foi submetida a uma biópsia, que confirmou o câncer do mesotélio. O médico receitou, então, Yervoy (ipilimubabe) para o tratamento da paciente.
Sim, a operadora é obrigada a custear o tratamento oncológico. Por isso, a paciente acionou o plano de saúde empresarial ao qual tinha direito exigindo o fornecimento do Yervoy. O pedido estava amparado por várias leis que protegem a saúde do consumidor. Conheça algumas delas:
– A Lei 9.656/98, que regula os planos de saúde, prevê a obrigatoriedade de cobertura de todas as doenças previstas na classificação da Organização Mundial de Saúde (OMS). O câncer de mesotélio está nesta listagem.
– O artigo 12 desta mesma lei determina que os planos forneçam os medicamentos e a cobertura de exames no controle da evolução de doenças, de acordo com a prescrição médica. Ou seja, se o médico receitou Yervoy, ele precisa ser custeado.
– O mesmo artigo prevê a cobertura para tratamentos antineoplásicos ambulatoriais e domiciliares de uso oral e procedimentos radioterápicos para tratamento de câncer.
Devido ao alto custo do remédio (uma ampola pode custar quase R$ 30 mil), os planos de saúde tentam se isentar da obrigação de fornecê-lo. Foi o que aconteceu com a paciente. A operadora se negou a custear o Yervoy, alegando que se trata de um medicamento off-label, ou seja, com prescrição diferente da que consta na bula do fármaco. Essa conduta é completamente abusiva. Entenda os motivos:
– A conduta da operadora gera danos ao consumidor, pois não há exclusão contratual para cobertura de tratamentos oncológicos, e distorce o contrato ao negar o tratamento prescrito pelo médico.
– O Recurso Especial n.º 668. 216 do Superior Tribunal de Justiça avaliou que um paciente não pode ser impedido de receber um tratamento com o método mais moderno possível no momento em que é diagnosticada a doença coberta pelo plano.
– A Súmula 102 do Tribunal de Justiça do Estado de São Paulo esclarece que, havendo indicação médica, é abusiva a negativa de cobertura de custeio de tratamento sob argumentos de que consiste num medicamento experimental ou não consta no rol de procedimentos da ANS.
Cabe lembrar ainda que a bula do fármaco Yervoy (ipilimumabe) tem, sim, a indicação para pacientes com mesotelioma maligno, em combinação com o nivolumabe, que também foi prescrito pelo médico da paciente. Além disso, o Yervoy é um remédio registrado pela ANVISA. E, ainda que conste na bula que uma medicação é destinada a determinada doença, outras podem se beneficiar dela também.
Após a recusa da operadora, a paciente entrou na Justiça para garantir seu direito à saúde e cobrar o atendimento obrigatório previsto no contrato.
Os documentos anexados à petição inicial deixaram claro a urgência do atendimento. O médico ressaltou o risco de rápida deterioração da saúde da paciente, devido ao comportamento agressivo dessa doença rara. De acordo com o INCA, mais de 80% dos óbitos ocorrem nos primeiros 12 meses.
Para não ser penalizado pela má-fé do plano, o paciente deve buscar o auxílio de advogados especialistas em direito à saúde. Justificativas como a desse caso são absurdas, e o paciente tem o direito de receber o tratamento, sobretudo pela garantia constitucional do direito à vida, como expresso no artigo 5º da Constituição Federal.
Se esse for também o seu caso, busque ajuda jurídica. No primeiro contato com a equipe que vai cuidar da sua ação contra a operadora, apresente, além de documentos pessoais, como identidade e CPF, comprovantes de pagamento do plano de saúde dos últimos três meses, os laudos e exames realizados durante o período de consultas, a prescrição médica, a bula do remédio, entre outros. Mensagens e e-mails que exibam a recusa da operadora também devem ser anexados.
Com o auxílio adequado, uma liminar pode ser deferida, obrigando o plano a fornecer de forma imediata e urgente o tratamento necessário. Cuide sempre da sua saúde!

Estadão | Thaís Manarini | 01/07/2023 | Rafael Robba
Queixas incluem negativas de cobertura de tratamentos, problemas para obter reembolsos e reajustes altos; entenda o que configura prática abusiva
Cerca de 50 milhões de brasileiros possuem planos de saúde – estima-se que, desse total de beneficiários, apenas 15% sejam idosos. Por outro lado, estudos indicam que esse grupo representa quase 30% da população que procura a Justiça contra as operadoras de saúde. Os números dão pistas, portanto, de que algumas práticas dessas empresas afetam especialmente os indivíduos mais velhos.
Para a advogada e cientista social Ana Carolina Navarrete, coordenadora do programa de Saúde do Instituto de Defesa do Consumidor (Idec), o cenário atual é diferente do que se via no passado. “Ocorria uma série de práticas abusivas, como permitir reajustes depois dos 70 anos”, exemplifica.
Após a publicação da Lei dos Planos de Saúde, em 1998, e do Estatuto do Idoso, em 2003, muitas dessas condutas foram revistas, favorecendo o consumidor. Porém, a advogada alerta que, hoje, há um tensionamento capaz de levar a retrocessos. Um dos principais problemas apontados nessa relação é a dificuldade enfrentada por quem tem mais de 60 anos em contratar os serviços da saúde suplementar.
O caminho até o contrato
“Não é um caminho fácil para o idoso ter um plano de saúde”, concorda Rafael Robba, advogado especialista em direito à saúde do Vilhena Silva Advogados, em São Paulo. O primeiro motivo para isso é a escassez de oferta de planos individuais/familiares – que é baseado em um contrato direto entre o beneficiário (pessoa física) e a operadora. Ele pode incluir só o indivíduo ou também seus dependentes.
Essas modalidades são mais reguladas pela Agência Nacional de Saúde Suplementar (ANS), que determina um teto de reajuste todos os anos, além de proibir o cancelamento do contrato sem que exista um motivo justo, como fraude ou inadimplência. No entendimento dos especialistas, essa maior proteção faz com que não haja muito interesse das operadoras em comercializar essa modalidade de plano – que seria justamente a ideal para quem tem mais de 60 anos.
Dessa maneira, às vezes o que sobra para a pessoa mais velha é o plano coletivo, que depende de um intermediário. Isto é: a contratação se dá entre a operadora de saúde e uma empresa, associação ou sindicato. “A questão é que, ao falarmos de um indivíduo idoso, ele não está necessariamente trabalhando ou tem um vínculo empregatício”, comenta Navarrete.
Diante desse cenário, o idoso acaba se filiando a alguma associação ou abre uma pequena empresa para, assim, ter acesso ao plano, no qual consegue incluir poucas pessoas. “A gente chama esse contrato de falso coletivo, porque, na verdade, quem contrata é a pessoa física mesmo”, comenta a advogada do Idec.
O problema é que essa modalidade não oferece tanta proteção ao consumidor. Ao contrário do que ocorre com os planos individuais/familiares, o valor do reajuste não é regulamentado pela ANS – e eles costumam ser mais elevados. Além disso, o contrato pode ser rescindido pela operadora sem motivo, basta que ela avise com 60 dias de antecedência. Na prática, as mesmas regras estipuladas para grandes corporações valem para os indivíduos que entram em um falso coletivo. “Os idosos ficam mais vulneráveis”, observa Robba.
Porém, os advogados comentam que, mesmo que o idoso decida optar por um plano coletivo, não é raro ele encarar obstáculos. “Podem receber informações rasas e objetivas das operadoras, como citar que não há interesse comercial no contrato”, diz Robba. “Elas não especificam que é por causa da idade, porque a conduta discriminatória seria clara. Mas, no caso a caso, a gente percebe que o fator decisivo foi a idade”, acrescenta o advogado, lembrando que essa conduta é mais frequente a partir dos 65 anos.
Para Robba, o ideal é registrar toda a comunicação com a operadora, desde o momento das negociações. “Se o consumidor perceber respostas muito evasivas, é possível buscar a Justiça para que a empresa aceite a contratação. Se o plano está à venda, e o idoso consegue pagar, não pode ser impedido”, afirma. A recusa é considerada ato discriminatório. O advogado aponta que, com a Lei dos Planos de Saúde, o Estatuto do Idoso e a própria Constituição Federal, o indivíduo mais velho está bem protegido nesse sentido. “E ele precisa saber disso”.
Os desafios para quem já tem plano
Para os idosos que pagam um plano de saúde, os advogados contam que um motivo recorrente de reclamações diz respeito à negativa de cobertura de determinados tratamentos – na verdade, essa é uma questão que respinga em todas as faixas etárias. “É um dos temas mais judicializados”, comenta Navarrete, destacando que essas recusas costumam ser indevidas e sem justificativa plausível.

Rafael Robba, especialista em Direito à Saúde
“As recusas acontecem sobretudo quando falamos de tratamentos mais caros. Só que a tendência é precisarmos de mais tecnologia no início e no fim da vida. São públicos que costumam demandar atendimentos complexos”, esclarece a advogada. Acontece que a operadora só pode negar a cobertura do tratamento se ele for considerado experimental ou ainda não tiver registro na Anvisa. “Fora isso, se o médico prescrever, a empresa precisa cobrir”, afirma Robba. “A recusa pode ser entendida como discriminação contra o idoso”, completa.
Na percepção da advogada do Idec, as operadoras precisam ter em mente que a mensalidade dos idosos já é mais elevada, porque há o entendimento de que eles podem vir a demandar mais do serviço mesmo. “Eles não pagam o mesmo que o jovem de 20 anos”, reforça. Portanto, não deveriam encontrar tanta burocracia ao precisar de algum tratamento específico.
O advogado aponta ainda que muitos idosos acabam utilizando o plano por meio de reembolso, mas recentemente eles têm encarado barreiras para usufruir do serviço. Para não ser surpreendido, Robba recomenda que, no momento da contratação, haja atenção especial nesse ponto – é importante entender, por exemplo, o limite de reembolso previsto no plano e como utilizá-lo. “Tem operadora exigindo uma série de documentos desnecessários, como extrato bancário para comprovar que o dinheiro saiu da conta do beneficiário. Isso é abuso”, afirma.
Mais um tópico sensível nessa relação diz respeito aos reajustes. Cabe lembrar que, no caso dos planos coletivos, os índices não são regulamentados pela ANS – então são superiores àqueles estipulados para os planos individuais/familiares. Fora isso, há readequação de valor por faixa etária, um cálculo que mudou ao longo dos anos.
Se o contrato for de antes de 1998, quando ficou estabelecida a Lei dos Planos de Saúde, vale o que está no documento. Caso o acordo tenha sido firmado entre 1998 e 2003, aí o aumento deve respeitar uma divisão por sete faixas etárias, sendo o último acréscimo permitido aos 70 anos – mas esse valor não podia ser seis vezes superior ao que se cobra da primeira faixa, entre 0 a 18 anos.
Com a publicação do Estatuto do Idoso, houve um avanço: depois de 2004, ficou estabelecido que os reajustes devem se basear em 10 faixas etárias, sendo que a dos 59 anos é a última suscetível ao aumento. Determinou-se ainda que a variação de preço acumulada nas três últimas faixas etárias não pode ser superior aos reajustes acumulados entre a primeira e a sétima faixas.
“Isso evita que as empresas abusem dos reajustes pouco antes de o indivíduo atingir a faixa dos 59 anos. É que muitas operadoras estavam fazendo justamente isso e, chegando na última faixa, não subiam tanto o valor para não ficar tão óbvio que era devido à idade”, conta Navarrete.
De qualquer maneira, somando os reajustes por idade, mais as adequações anuais de preço, não é incomum que o indivíduo mais velho se veja diante de uma mensalidade alta. “Mas a legislação entende que, se o valor for excessivo, e representar uma barreira para a pessoa permanecer no plano, isso pode ser questionado judicialmente”, informa Robba. Caso o consumidor se sinta lesado por alguma prática, pode procurar, antes, a ANS, o Procon ou o Idec.
Mudança na pirâmide etária exige transformações
Com o crescimento da população idosa, os especialistas entendem que é urgente levantar o debate sobre como atender melhor esses indivíduos – e não como excluí-los. “Muitas vezes, o tom da conversa das operadoras é no sentido de achar maneiras de aumentar a mensalidade do idoso, com base no argumento de que ele custa caro. Ignora-se o fato de que essa pessoa já paga a mais pelo plano”, critica Navarrete. “Não dá para desenhar o mercado para atender só jovens e saudáveis”.
Para ela, é fundamental ainda pensar em estratégias de prevenção, para dar apoio à população que está envelhecendo – e em ritmo acelerado. “O foco da saúde suplementar, hoje, é no atendimento depois que a pessoa adoeceu, não é antes. O mercado faz assistência, e não prevenção. Depois, as operadoras reclamam do alto custo. Mas o sistema é todo pensado para fornecer o mais caro”, diz.
A visão das operadoras
Procurada pelo Estadão, a Federação Nacional de Saúde Suplementar (FenaSaúde), representante de 13 grupos de operadoras de planos de saúde, informa que suas associadas seguem estritamente as normas da Agência Nacional de Saúde Suplementar (ANS) no que diz respeito à oferta de planos de saúde para todas as faixas etárias, sem qualquer restrição ao ingresso de beneficiários por conta de idade.
A nota diz que, além disso, cumprem rigorosamente as regras sobre reajuste de mensalidades e reembolso, estando sujeitas à fiscalização da agência e passíveis de punição em caso de descumprimento.
“Vale ressaltar que, segundo levantamento realizado pela ANS e divulgado com exclusividade pelo próprio Estadão, a faixa de beneficiários que mais cresce nos planos de saúde é justamente a dos idosos – como resultado esperado do processo de envelhecimento populacional por que passa o Brasil. Entre 2013 e 2023, o total de pessoas com mais de 60 anos nos planos de saúde aumentou 32,6%, enquanto a alta no total de beneficiários foi de apenas 5,3%. Entre os idosos de 70 a 74 anos o avanço foi ainda mais contundente, de 41,9%”.

Migalhas | 15/06/2022 | Fábio Pereira dos Santos
Plano de saúde é condenado a cobrir medicamento IDHIFA (enasidenib) sem registro na Anvisa: Decisão é do Tribunal de Justiça de São Paulo que, aplicando a técnica do distinguishing, afastou a aplicabilidade da tese firmada pelo Superior Tribunal de Justiça no Tema 990.
Dentre os temas mais judicializados no âmbito dos contratos de plano de saúde, certamente estão as demandas dos consumidores pelo custeio de medicamentos prescritos para o combate de doenças graves.
São diversas as justificativas das operadoras para negar o custeio de medicamentos prescritos aos consumidores, como “ausência de previsão do rol da ANS”, “uso off-label (fora da bula)” e “ausência de registro da ANVISA”.
E foi com base em entendimento majoritário da 2ª Seção do Superior Tribunal de Justiça (STJ), em 2018, que foi fixada a tese vinculante intitulada como “Tema 990”, oriunda do julgamento dos REsp 1712163/SP e REsp 1726563/SP sob o rito dos recursos repetitivos (art. 1.036 do CPC).
A tese firmada pelo STJ no Tema 990 determinou que “As operadoras de plano de saúde não estão obrigadas a fornecer medicamento não registrado pela ANVISA”, com lastro principalmente no risco sanitário de permitir a circulação de medicamentos cuja eficácia, segurança e qualidade não tenham sido atestadas pela agência reguladora.
Entretanto, em recente julgamento do recurso de apelação 1003967-58.2018.8.26.0114, a 8ª Câmara de Direito Privado do Tribunal de Justiça de São Paulo (TJ/SP), decidiu, à unanimidade, condenar a operadora de plano de saúde ao custeio de medicamento importado, sem registro na ANVISA, ao realizar distinção do caso concreto com a tese vinculante firmada no Tema 990/STJ.
O tribunal decidiu que a ratio decidendi existente no julgamento dos recursos repetitivos se diferenciava do caso da beneficiária paulista, já que a droga por ela necessitada possui ínfimas chances de ser submetida a registro perante a Agência Nacional de Vigilância Sanitária.

Advogado Fábio Santos
E isto porque, a droga necessitada pela consumidora foi criada especialmente para combater doença rara, isto é, que atinge pequena parcela da população, fato que demonstra pouco ou nenhum interesse comercial da indústria farmacêutica em pedir o seu registro no país.
Por outro lado, a droga em discussão já tinha, desde 2017, registro em renomado órgão dos Estados Unidos da América (FDA – Food and Drugs Administration), que atestou a eficácia do medicamento IDHIFA® (enasidenib) no combate à mutação patogênica “IDH2”.
A aplicação da técnica de distinguishing adotada pela corte paulista também se baseou em precedente do STJ no julgamento do REsp 1.885.384/RJ, de relatoria do ministro Paulo de Tarso Sanseverino, no qual foi reconhecida excepcional obrigação das operadoras de plano de saúde no custeio de medicamentos importados, desde que haja “eficácia e segurança comprovadas, mas ainda sem registro na ANVISA, nos casos de doenças raras e ultrarraras.”
Esta nova vertente jurisprudencial, ainda que tardia, espelha uma análise mais aprofundada pela corte de uniformização ao julgar casos tão delicados e que influenciam diretamente na proteção daquele que é um dos mais valiosos bens jurídicos tutelados, o direito à saúde.
Na verdade, a abertura de exceções para reconhecer o dever de custeio de medicamentos importados já existe no âmbito das demandas contra o SUS, porquanto o Supremo Tribunal Federal (STF), no julgamento do “Tema 500” (RE n.º 657718), já havia estabelecido que, estando presentes três requisitos, é possível a cobertura de medicamentos importados, são eles:
(i) a existência de pedido de registro do medicamento no Brasil (salvo no caso de medicamentos órfãos para doenças raras e ultrarraras);
(ii) a existência de registro do medicamento em renomadas agências de regulação no exterior;
(iii) a inexistência de substituto terapêutico com registro no Brasil.
A novidade é que a decisão proferida pelo TJ/SP reconhece a aplicabilidade dos 3 requisitos também às demandas em que o beneficiário postula a cobertura de seu tratamento contra a operadora de plano de saúde, e não apenas contra o Poder Público.
A bem da verdade, reconhecer a substancial diferença entre a tese adotada no julgamento do Tema 990/STJ e o caso da parte que pleiteava o fornecimento de seu medicamento, demonstra a coerência do TJSP no que concerne aos direitos fundamentais da ampla-defesa e do contraditório.
É certo que o sistema de precedente qualificados instituído pelo Novo Código de Processo Civil (NCPC) demonstra uma tentativa da Lei Adjetiva de otimizar a jurisprudência, buscado a uniformização do entendimento dos tribunais quando forem submetidas a julgamento questões repetitivas.
No entanto, a própria percepção de “recursos repetitivos” traz obrigatoriedade de se ter questões jurídicas idênticas, já que o entendimento vinculante é firmado com base em situação específica apresentada ao judiciário, não abarcando diferenciações substanciais que possam surgir nos litígios.
O Tema 990/STJ demonstra que não houve abrangência da situação jurídica da consumidora paulista em seu julgamento e este aspecto está presente na própria ausência de qualquer consideração feito pelo STJ sobre doenças raras e drogas órfãs ao definir a tese repetitiva.
Ademais, a decisão de cunho repetitivo, ao se replicar sem nenhuma distinção fática sobre outras demandas propostas no judiciário, acaba por causar injustiça ao jurisdicionado, pois como explica Marinoni1: “obviamente não se pode dizer amém a um procedimento que, embora dotado da elogiosa ambição de dar otimização à resolução das demandas, viola o direito fundamental de ser ouvido e de influenciar o juiz.”
É no exercício do contraditório e da ampla defesa que o jurisdicionado tem a oportunidade de influenciar a decisão judicial sobre sua pretensão, sendo vedado que se tolha essas garantias constitucionais em detrimento de uniformização de uma jurisprudência vinculante indistinta, como ocorreu no julgamento do Tema 990/STJ.
Foi com base nessas premissas que o TJSP, sensível aos argumentos da parte, que demonstraram a distinção de sua situação jurídica com aquela decidida no âmbito do Tema 990/STJ, reconheceu a excepcional obrigação da Operadora de plano de saúde a custear medicamento importado, cuja utilização não demonstra risco sanitário.
Portanto, ainda que haja a obrigação legal (art. 927, III do CPC) dos tribunais estaduais aplicarem as teses firmadas em sede de recursos repetitivos, não se pode perder de vista que a tutela jurisdicional, sobretudo, deve ser prestada em observância à correta aplicação das normas de direito às situações fáticas e jurídicas apresentadas, o que pode atrair, a exemplo do julgado do TJSP, mitigação da jurisprudência vinculante para evitar injustiças.
Medicamento Zolgensma é vendido por mais de US$ 2 milhões; no Brasil, porém, foi estipulado preço máximo de R$ 2,8 milhões, o que leva a impasse com fabricante
São Paulo | A Justiça Federal em Pernambuco determinou neste sábado (18) que o Ministério da Saúde forneça o medicamento zolgensma —conhecido como o remédio mais caro do mundo— ao bebê, de quatro meses, Benjamin Brener Guimarães.
Ele foi diagnosticado com AME (atrofia muscular espinhal) tipo 1, considerado o mais grave, aos três meses, no dia 23 de agosto.
Zolgensma, da Novartis, considerado o remédio mais caro do mundo – Bruno Santos – 24.ago.2020/Folhapress
Desde então, seus pais, Túlio Guimarães, 45, e Nathalie Brener Guimarães, 34, iniciaram uma campanha para arrecadar US$ 2,125 milhões, o equivalente a mais de R$ 11 milhões. Com o valor, eles pretendiam importar dos EUA a dose única do zolgensma, do laboratório Novartis Biociências S.A.
A decisão foi proferida, em tutela de urgência, pela juíza federal Joana Carolina Lins Pereira, titular da 12ª Vara. A União precisa cumpri-la num prazo de 20 dias.
A Justiça também ordenou que a família do bebê informe em cinco dias o valor arrecadado nas campanhas para a compra do medicamento. O governo federal deverá custear o restante.
Até a sexta-feira (17), o valor ultrapassava R$ 3,4 milhões. Como o Ministério da Saúde pode recorrer da decisão, a família manterá a campanha nas redes sociais.
“Esse medicamento é uma terapia diferente da disponibilizada atualmente, porque corrige o defeito principal da doença e não faz um trabalho paliativo”, conta o pai do bebê.
“Que o governo se sensibilize e coloque à disposição esse medicamento, porque pode salvar a vida de uma criança e diminuir o sofrimento que passei e estou passando com a minha família e as outras famílias também. Eu quero curar meu filho e fazer com que as pessoas saibam mais sobre o que é a AME”, completa.
Benjamin não é o único bebê a lutar pelo tratamento. Segundo Fátima Braga, presidente da Abrame (Associação Brasileira de Amiotrofia Espinhal), atualmente, no país, ao menos 30 crianças estão em campanha nas redes sociais com o objetivo de arrecadar fundos para a importação do zolgensma.

Rafael Robba – Vilhena Silva Advogados.
Mas esse número pode ser maior. “Ainda há famílias que não possuem acesso a redes sociais nem o médico que conheça a doença e prescreva o medicamento”, alerta.
Em agosto de 2020, a Anvisa (Agência Nacional de Vigilância Sanitária) aprovou o registro do zolgensma para o tratamento do tipo 1, em crianças de até 2 anos, no Brasil.
O acesso à droga ficou mais fácil graças à decisão da CMED (Câmara de Regulação do Mercado de Medicamentos), órgão interministerial responsável pela definição dos preços máximos de comercialização de remédios no país.
Assim, conforme a CMED definiu em dezembro do ano passado, o zolgensma não pode custar mais que R$ 2.878.906,14 no Brasil.
A farmacêutica Novartis entrou então com um processo pedindo uma adequação do preço e criou um impasse.
“A solicitação de precificação feita pela Novartis pautou-se no fato de o zolgensma ser uma terapia gênica inédita para a indicação, com o potencial de responder às necessidades não atendidas de AME, oferecendo aos pacientes claros benefícios clínicos no tratamento, resultados duradouros e com bom perfil de segurança”, afirma o laboratório, em nota.
“A empresa segue em busca de uma equalização entre a viabilização de novas tecnologias e uma precificação que seja condizente com as características técnico-científicas das novas terapias”, escrevem ainda.
O texto diz também que, enquanto houver a rediscussão do preço junto à CMED, não é possível a aquisição do produto em território nacional por meio da Novartis Brasil. A informação foi repetida pela assessoria de imprensa do laboratório, por telefone.
A reportagem questionou a Anvisa. Ao contrário do que afirma a Novartis, de acordo com a agência, a comercialização do zolgensma está liberada, independentemente do pedido de reconsideração por parte da empresa interessada.
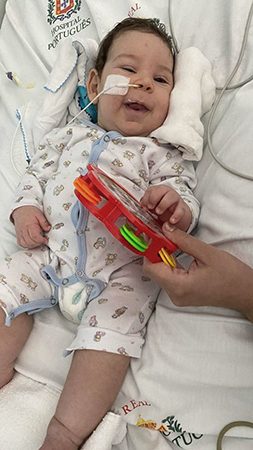
Benjamin Brener Guimarães, de 4 meses, foi diagnosticado com AME (Atrofia Muscular Espinhal) tipo 1; sua família faz campanha para arrecadar R$ 11 milhões para a importação do zolgensma – Arquivo de família
“Não há um prazo fechado para a decisão final, porém, a empresa pode comercializar a qualquer momento, não precisa aguardar a decisão final. Está valendo o preço de R$ 2,8 milhões”, afirma a Anvisa.
“Esse é o fundamental papel da CMED: defender o povo brasileiro. As regras para precificar são públicas. Ela não age ao arrepio da lei. A negociação ocorre à luz do sol no interesse da cidadania, do acesso aos medicamentos”, defende o médico sanitarista e professor de saúde pública da USP Gonzalo Vecina Neto, ex-presidente da Anvisa.
Rafael Robba, advogado especialista em direito à saúde e sócio do escritório Vilhena Silva Advogados, entende que o fabricante pode não comercializar o medicamento zolgensma no país enquanto discutir o preço. Porém, ele alerta, os planos de saúde devem oferecer cobertura, porque o medicamento já está registrado no país.
“A legislação diz que os medicamentos de uso hospitalar têm cobertura obrigatória. Os planos se negam a cobrir por vários motivos, mas principalmente por causa do custo elevado. Isso faz com que os pacientes tenham que buscar a Justiça”, explica.
“Como as pretensões estão muito distantes —a Novartis querendo comercializar por mais de R$ 11 milhões e a Anvisa por R$ 2,8 milhões—, eu acho que precisa de uma atuação mais efetiva da Anvisa no sentido de tentar negociar e conciliar um meio-termo para que o paciente tenha acesso à medicação. O que também não pode é prolongar tanto esta discussão”, afirma.
O zolgensma pode melhorar a sobrevivência dos pacientes, reduzir a necessidade de ventilação permanente para respirar e alcançar marcos de desenvolvimento motores.
Em 7 de agosto do ano passado, a bebê Marina Moraes de Souza Roda, que completou 3 anos em 1º de setembro, foi a primeira criança a receber a dose única da medicação no país. O procedimento ocorreu no Hospital Israelita Albert Einstein, no Morumbi (zona sul).
Renato Moraes de Souza, pai de Marina, comemora o progresso diário. “Depois do medicamento zolgensma, ela consegue fazer muitos movimentos novos, teve ganho de força e a questão respiratória também está estável e em progresso. Além da medicação, ela continua com as fisioterapias e tratamentos extras, o que é muito importante para a evolução da criança”, afirma.
A atrofia muscular espinhal é causada por uma alteração do gene responsável por codificar a proteína necessária para o desenvolvimento adequado dos músculos. A doença é rara e provoca fraqueza, hipotonia, atrofia e paralisia muscular progressiva, afetando a respiração, a deglutição, a fala e a capacidade de andar.
Os principais sinais e sintomas são perda do controle e das forças musculares e a incapacidade ou dificuldade para engolir, segurar a cabeça, respirar e realizar movimentos de locomoção.
Quanto mais cedo diagnosticada a doença e mais breve a medicação para controle for iniciada, melhor o prognóstico.
Em maio deste ano, foi sancionada a lei n.º 14.154, que amplia de seis para 50 o número de doenças rastreadas pelo teste do pezinho oferecido pelo SUS (Sistema Único de Saúde). A ampliação será de forma escalonada e estabelecida pelo Ministério da Saúde. A AME estará na última etapa.
A lei entrará em vigor um ano após a publicação, de acordo com o próprio ministério.
Fonte: Folha de S. Paulo | Patrícia Pasquini | 20.09.2021
Conteúdo relacionado
Oncologia Brasil | 28.06.2021 | Dr. Cesar Costa Read more »

Após realizar diversas abordagens terapêuticas, a paciente diagnosticada com câncer de mama com metástase óssea recebeu prescrição médica para uso do medicamento Piqray (Alpelisibe). Como se não bastasse todo o desgaste emocional e a luta contra o câncer de mama, a paciente enfrentou também uma dura batalha contra o plano de saúde. Entenda o caso.
Veja Saúde | Chloé Pinheiro | 10/03/2021 Read more »

Plano de saúde se recusa a fornecer medicamento quimioterápico importado, sob argumento de exclusão contratual. Embora o medicamento Tiotepa (Tepadina) ainda não tenha sido registrado na Anvisa, tampouco incluído no Rol da ANS, a Justiça entendeu que o plano de saúde deveria custear integralmente o tratamento. Entenda o caso.
O quadro clínico delicado da paciente, de apenas 6 anos, diagnosticada com neuroblastoma, teve que ser levado ao Judiciário para discussão. Isso porque, o plano de saúde se recusou a fornecer o medicamento Tiotepa (Tepadina), imprescindível na realização do transplante de medula óssea prescrito pelo médico.
Após receber o diagnóstico de neuroblastoma, um tipo de câncer raro e agressivo, a garota iniciou o tratamento quimioterápico. Porém, as chances de cura com as drogas convencionais não ultrapassam os 40%, razão pela qual o médico que acompanha a paciente prescreveu o transplante de medula óssea.
O protocolo prescrito pelo médico consiste na realização de dois transplantes autólogos de medula óssea, o primeiro associado à utilização de Tiotepa e Ciclofosfamida, seguido pelo segundo transplante com a utilização de Carboplatina, Etoposide e Melfalano. Sendo assim, o primeiro transplante depende do suporte do medicamento Tiotepa para possibilitar a realização do segundo, e assim dar continuidade ao tratamento.
Apesar de toda terapêutica, inclusive o transplante de medula óssea ter sido autorizado pelo plano de saúde, o medicamento Tiotepa (Tepadina) foi negado, sob argumento genérico de exclusão contratual. Sem o medicamento, o transplante não poderia ser realizado e a paciente corria risco iminente de vida pelo avanço da doença.
Sem dúvida, a negativa de cobertura e a cláusula contratual que exclui o medicamento é considerada abusiva. Além disso, a negativa de cobertura afronta a Lei 9656/98, bem como as Súmulas 95 e 102 do Tribunal de Justiça de São Paulo.
Importante esclarecer que, embora o medicamento Tiotepa ainda não tenha sido registrado na Anvisa, há expressa autorização do órgão sanitário para importação do fármaco, em caráter excepcional, por meio da Resolução n.º 28/2008 e da Instrução Normativa 1/2014.
A lista de medicamentos liberados para importação pela Anvisa, em caráter excepcional, leva em consideração a existência de monografias baseadas em estudos oficiais dos países onde são fabricados, indicando a eficácia e segurança desses produtos.
Diante da negativa e necessidade de realizar o transplante de medula óssea com urgência, não restou outra alternativa a família, senão ingressar com uma ação judicial para garantir a sobrevida da criança.
Definitivamente, o pedido de liminar precisava ser eficaz. Nesse caso, a paciente foi representada pelo escritório Vilhena Silva Advogados, que através do pedido de liminar, exigiu que o plano de saúde custeasse o medicamento Tiotepa, conforme prescrito pelo médico, até alta médica definitiva. Assim como, o pedido de prioridade de tramitação, tendo em vista a gravidade da doença.
Ao analisar o caso, o juiz da 3ª Vara Cível do Foro Regional XI – Pinheiros da Comarca de São Paulo, entendeu que o plano de saúde deveria custear integralmente o medicamento Tiotepa, conforme prescrição médica.
O magistrado ressaltou que a questão se encontra pacificada no Tribunal de Justiça de São Paulo, conforme a Súmula 95 e 102: “Havendo expressa indicação médica, não prevalece a negativa de cobertura do custeio ou fornecimento de medicamentos associados a tratamento quimioterápico.” e “Havendo expressa indicação médica, é abusiva a negativa de cobertura de custeio de tratamento sob o argumento da sua natureza experimental ou por não estar previsto no rol de procedimentos da ANS”.
Desse modo, amparada pela liminar concedida, a criança pôde dar continuidade ao tratamento e realizar o transplante de medula óssea. Fique atento aos seus direitos. Se houver qualquer negativa por parte do seu plano de saúde, converse com advogados especialistas na área de direito à saúde e lute pelo medicamento prescrito pelo seu médico.
